背景介绍
细菌感染,尤其是耐药菌感染和生物膜相关感染,始终是临床治疗中的难点。与游离细菌不同,生物膜中的细菌被胞外聚合物基质紧密包裹,不仅显著阻碍抗菌药物渗透,还会增强细菌对抗生素和宿主免疫清除的耐受性,导致感染迁延不愈,严重时可引发组织损伤甚至全身性感染。现有治疗方式仍以抗生素为主,但在耐药性持续加剧、生物膜屏障普遍存在的背景下,传统治疗策略越来越难以满足临床需求。如何突破生物膜屏障、实现感染部位的精准激活和高效清除,已成为抗感染研究的重要科学问题。
近日,中国医学科学院生物医学工程研究所整合再生医学实验室戴建武教授、阴慧娟研究员和董晓曦副研究员为共同通讯作者在国际知名期刊 Carbohydrate Polymers上发表题为“Hyaluronic acid-engineered infection-responsive liposomes achieve biofilm penetration and synergistic photothermal-photodynamic antibacterial therapy”的研究论文。该研究围绕“如何让材料在感染部位被激活,并与光疗设备协同实现高效抗感染”这一问题,该研究构建了一种透明质酸修饰的感染响应型脂质体平台 HA@ICG@Lip,在感染微环境中可被激活增强材料对细菌的黏附和对生物膜的深部穿透能力。在此基础上,团队结合自研808 nm LED 光疗装置,利用 ICG 在近红外照射下同时产生活性氧和局部热效应,实现了光动力与光热的协同抗菌治疗。曹士盛硕士研究生为论文第一作者。

文章详细介绍
近年来,光疗因其不依赖传统抗生素靶点、可实现时空精准调控等优势,在抗感染领域显示出良好应用前景。其中,吲哚菁绿(ICG)兼具光热和光动力双重治疗潜力,可在近红外照射下产生活性氧和局部热效应,实现细菌杀伤和生物膜破坏。然而,ICG 光疗效果高度依赖于两个关键条件:一是光敏材料能否在感染部位稳定富集并深入生物膜内部;二是能否提供与其近红外吸收特性相匹配、输出稳定且具有临床应用潜力的光源。现有研究中,ICG光疗多依赖激光光源,但激光设备通常存在成本较高、照射面积有限、光斑均一性不足、局部热积累明显以及器械化和临床普及难度较大等问题,其与材料性能之间的协同设计也仍显不足。对于 ICG 这类近红外光敏体系而言,理想光源不仅需要在 808 nm 波段提供有效激发,还应兼顾照射均一性、热量可控性、器械集成性和实际应用可及性。
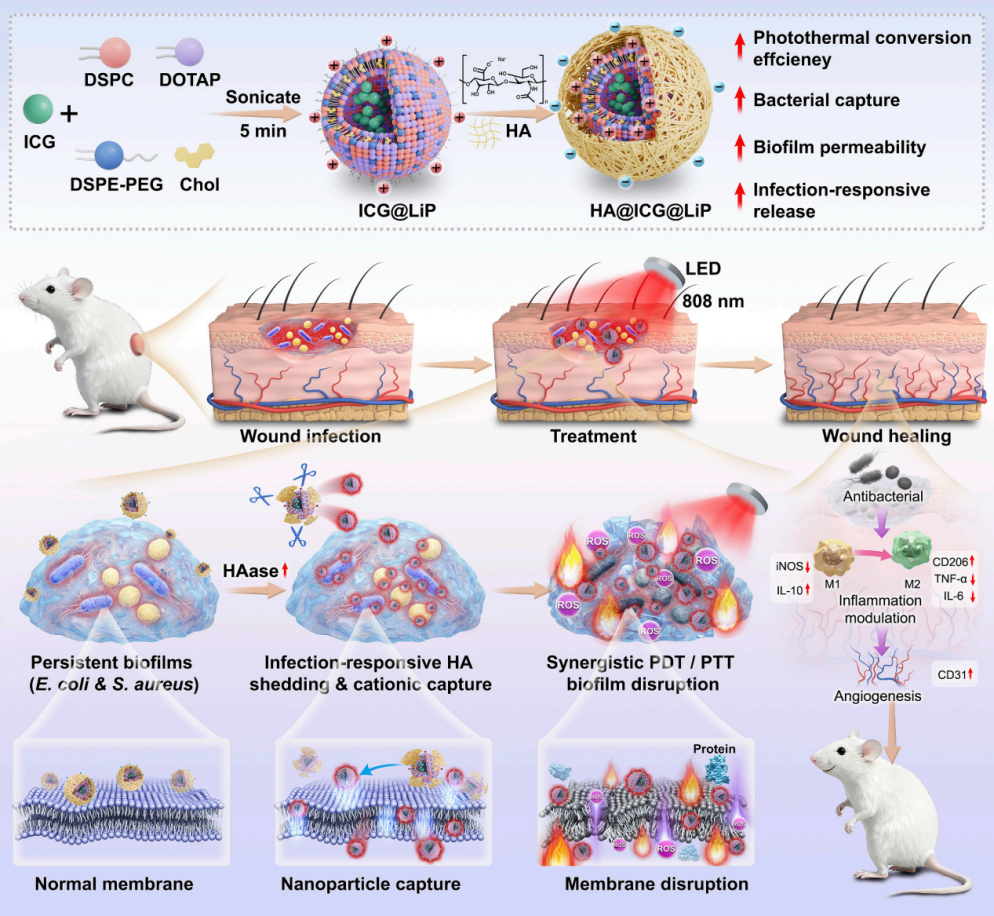
图1:HA@ICG@Lip纳米平台设计的示意图及其感染响应性抗菌机制,包括透明质酸酶触发的去屏蔽、增强的生物膜穿透、细菌捕获以及协同光热/光动力治疗。
在具体设计上,团队围绕感染治疗中的两个核心障碍——“进不去”和“杀不透”——进行了针对性设计。一方面,研究团队利用透明质酸(HA)作为外层功能屏蔽层,使脂质体在非感染环境下保持相对稳定和低非特异相互作用;另一方面,在感染相关微环境中,局部升高的透明质酸酶(HAase)能够逐步降解HA层,诱导脂质体发生“去屏蔽”转变,暴露出带正电的脂质体核心,从而增强其与带负电细菌表面的黏附,并促进其向生物膜深层渗透。
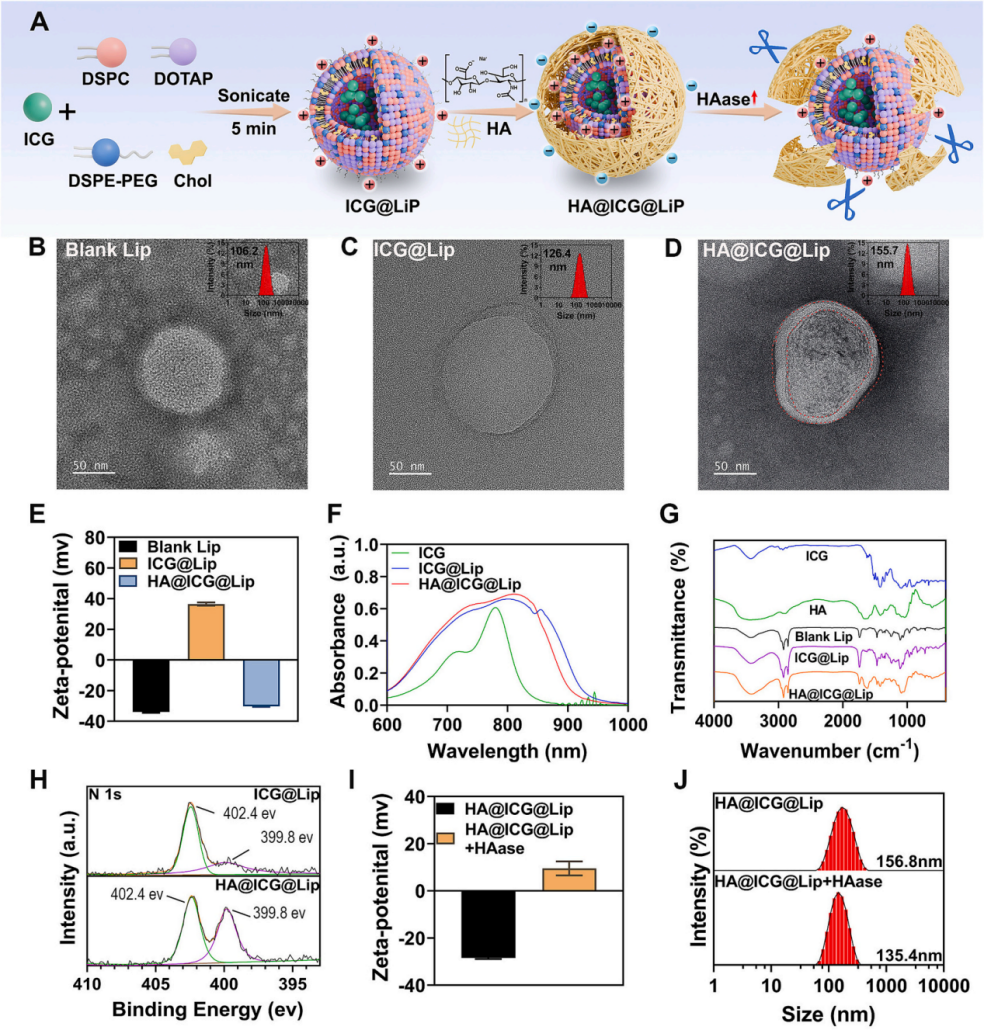
图2:HA@ICG@Lip纳米平台的合成与表征。
与此同时,研究团队还发现,吲哚菁绿(ICG)在脂质体微环境中形成了J聚集结构,可增强近红外吸收并提高光热转换能力,为后续光疗增效提供了材料基础。
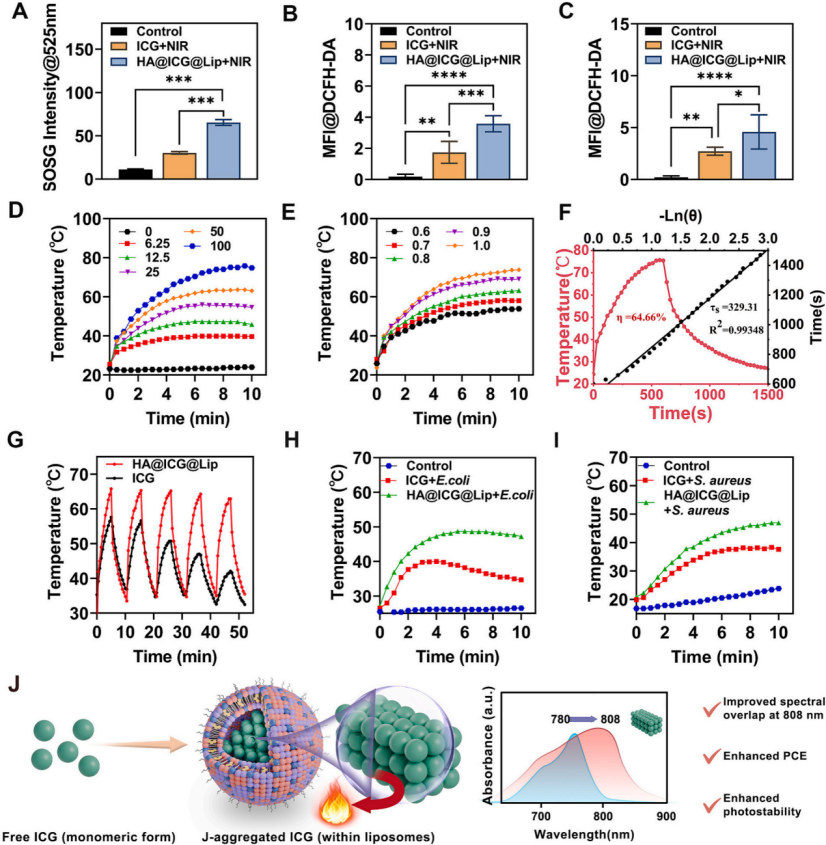
图3:HA@ICG@Lip具有高光热转换效率和增强的光稳定性,这些特性与ICG在脂质体双分子层内形成J-聚集体有关。
体外生物膜研究表明,HA@ICG@Lip 可在大肠杆菌和金黄色葡萄球菌混合生物膜中发生 HA 外壳的特异性降解,暴露带正电的脂质核心,从而增强细菌黏附与局部富集。经 808 nm 光照后,该体系同步产生活性氧和局部高热,诱导 PDT/PTT 协同效应,显著破坏细菌细胞膜及生物膜结构,最终实现细菌杀灭和生物膜解体
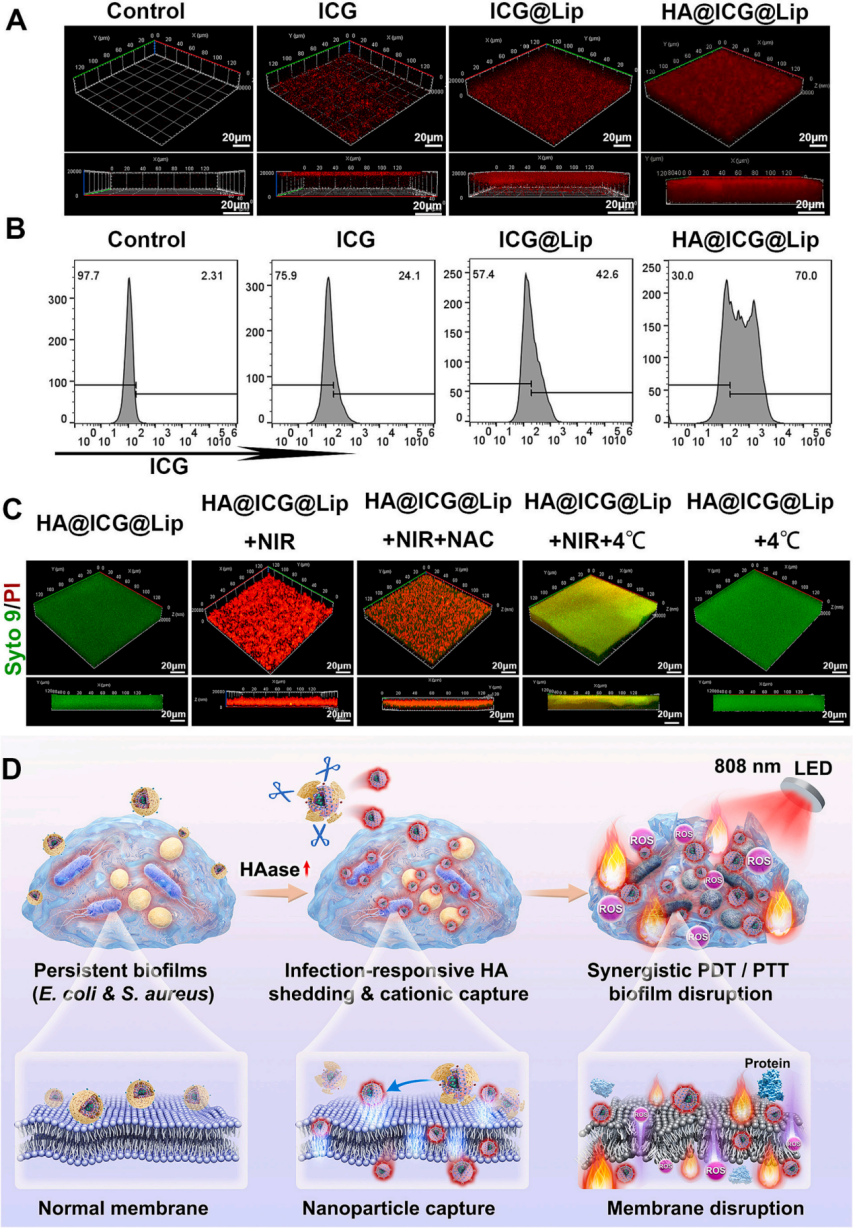
图4:HA@ICG@Lip实现了增强的生物膜穿透和细菌捕获,并且在近红外照射下发挥了光热和光动力联合抗生物膜的作用。
在体内感染创面模型中,HA@ICG@Lip结合 808 nm LED 照射后,能够显著减少创面细菌负荷,减轻局部炎症反应,并加快伤口闭合和组织修复。相比单纯依赖药物杀菌的传统方式,这一体系实现了从“感染响应激活”到“生物膜穿透”,再到“光热/光动力协同清除”的连续治疗过程,体现出材料设计与光疗设备协同工作的优势。值得注意的是,团队在研究中所采用的LED光源具有成本低、照射均一、热效应可控和器械化潜力强等特点,更适合感染创面等实际应用场景,也使该工作不仅停留在材料层面的创新,同时兼具一定的器械转化特色。
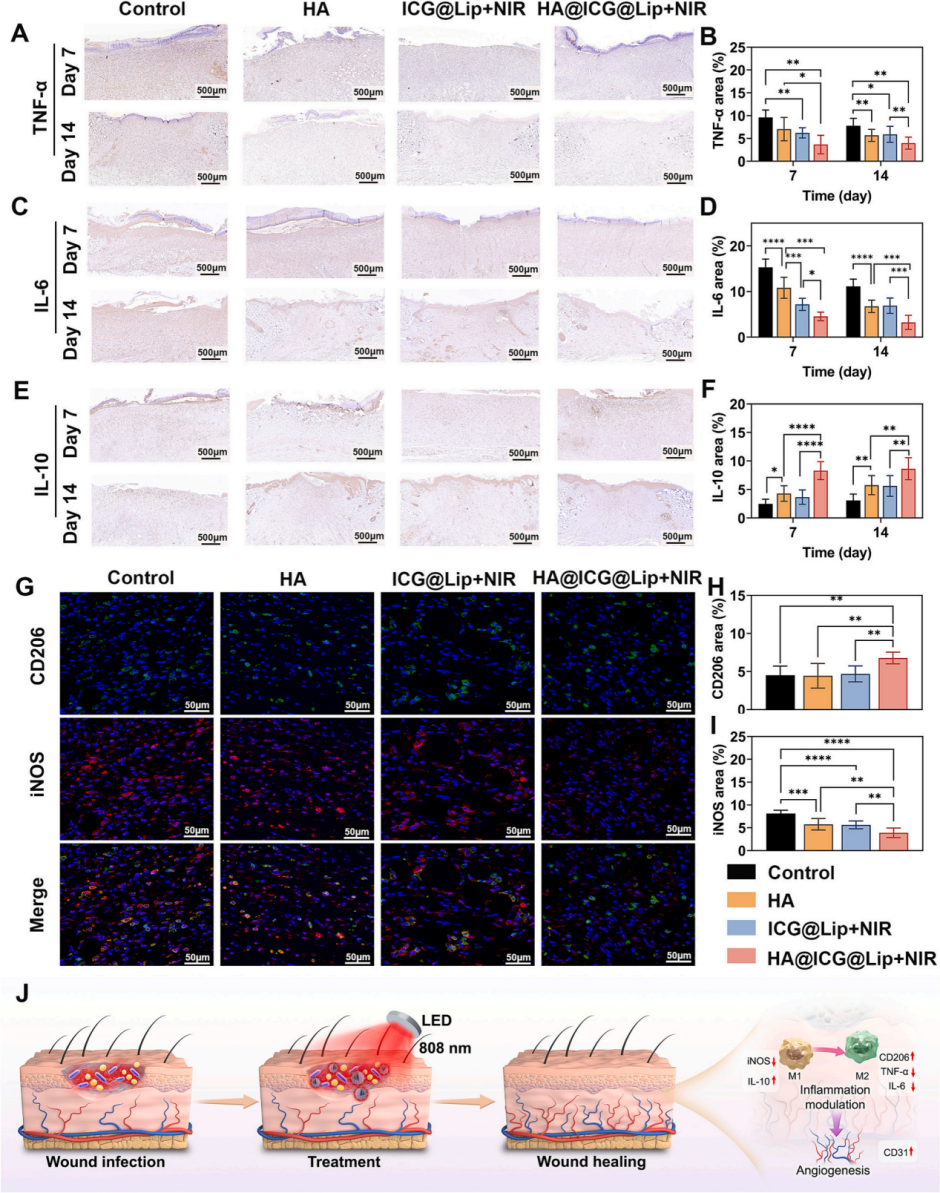
图5:HA@ICG@Lip结合 808 nm LED 照射可促进感染伤口愈合并调节炎症反应。
该研究的意义在于,它提出了一种面向复杂生物膜相关感染的新型解决思路:不再单纯依赖抗生素,而是通过感染微环境响应型材料与近红外光疗设备的协同设计,实现材料在病灶处的精准激活、深部生物膜穿透和高效联合杀菌。这一成果不仅为感染性创面治疗提供了新的技术方案,也为先进医用材料与医疗器械的交叉融合提供了有代表性的研究案例。
参考文献
Shisheng Cao, Zeqi Liu, Jiakang Zhao, Xiaoxi Dong, Jianwu Dai, Huijuan Yin. Hyaluronic acid-engineered infection-responsive liposomes achieve biofilm penetration and synergistic photothermal-photodynamic antibacterial therapy. Carbohydrate Polymers,2026,383:125313.
全文链接:https://doi.org/10.1016/j.carbpol.2026.125313
作者简介:

戴建武,博士,研究员,博士生导师。
主要研究方向:研究磁、声、光、电等物理信号对组织器官发育及再生的影响,探索物理信号对组织器官发育与再生的作用机制。通过整合物理信号与化学信号的作用,建立引导组织器官再生的微环境,研发组织器官再生的新技术、新产品。
代表性成果:
1.突破了再生医学关键技术。研发了系列具有自主知识产权的再生医学产品。研发的基于胶原蛋白特异结合的BMP2活性骨材料成功获得创新医疗器械注册证,实现了0-1的突破。提出组织内源干细胞的激活与分化是组织再生的重要机理。率先成功组织了包括子宫内膜再生、卵巢再生、脊髓损伤再生,心肌再生等多个产品的临床研究。
2.研发的子宫内膜再生修复产品为子宫内膜损伤的不孕患者提供了一种有效的治疗手段,入选2014年中央电视台年度科技创新人物;卵巢再生修复取得突破,第一个卵巢早衰患者2018年1月12日诞生世界上首位健康宝宝。子宫内膜再生卵巢再生及脊髓损伤再生成果入选国家改革开放40周年创新成果展。
3.成功研发了首个脊髓损伤再生修复产品NeuroRegn支架。NeuroRegn支架2014年开始临床研究,长期的临床随访结果表明NeuroRegn支架治疗急性及陈旧性脊髓损伤安全有效。研究团队成为国际上最受关注的脊髓损伤再生修复研究团队之一。

阴慧娟,研究员,硕士生导师。
郑州大学临床医学专业本科学位,中山大学生物医学工程专业硕士学位,天津医科大学生物医学工程专业博士学位,瑞典皇家理工学院访问学者。中华医学会激光医学分会委员,中国抗癌协会肿瘤光动力专委会常委,天津市医学会激光医学分会副主任委员,中国人体健康科技促进会第五届理事会理事。
研究领域:目前在戴建武所长的整合再生医学课题组从事光医学的基础和应用研究。致力于研究光动力疗法的新技术和装备研究以及光调控组织器官再生方面的研究。代表性成果包括光动力胶囊微机器人技术、循环光动力技术、幽门螺杆菌光疗技术、光刺激促进伤口愈合、光调控阿尔兹海默症、肠道菌群光生物调节、光调控脊髓损伤等。其中光动力胶囊微机器人技术已经形成3类胶囊样机,光刺激促进伤口愈合实现成果转化,研发出多波长伤口愈合光疗仪。
主要业绩:主持并参与主持/参加国家自然科学基金项目4项,科技部项目5项,天津市卫计委项目1项,天津市重点研发计划项目1项,医科院创新工程人工智能专项1项,其他院校级项目4项,横向合作课题十余项,完成成果转化3项。发表一作/通讯作者SCI论文25篇,参与专著2部,授权专利19项。

董晓曦,副研究员,北京协和医学院博士,
中国医学科学院生物医学工程研究所整合再生医学实验室骨干成员。
长期从事光医学基础与应用研究,聚焦神经组织光场分布、光医学临床应用基础、人工智能医学建模及激光医学相关设备研发。当前重点研究物理因子调控神经组织损伤修复中的组织内能量场精确控制,以及光、声、电、磁等物理因素在组织内能量递送的数学建模与优化。主持国家自然科学基金等多项科研项目,获授权专利11项,实现专利转化1项。
撰稿:阴慧娟
编辑:李梓萌
运营:崔 畅
审核:杨桦 黄鹏羽
 电话:022-87890296
电话:022-87890296  传真:022-87890296
传真:022-87890296
